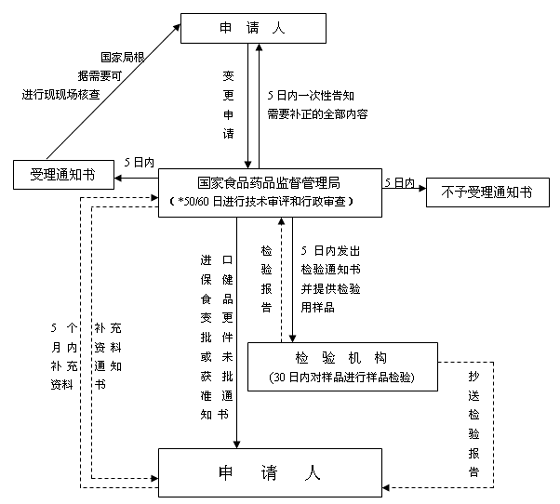
对改变产品规格、质量标准以及进口保健食品生产厂商在中国境外改变生产场地的变更申请(进口)
时间:2022-02-19 浏览:2,007
导读:
* 需要补充资料的注册申请,其审查时限在原审查时限的基础上延长10日。
延长审查时限,从收到最后一次补充资料之日起开始计算。
|
|||
责任编辑:本站小编
相关文章:
- [流程周期]保健食品原注册人产品转备案流程
- [流程周期]进口保健食品备案申请条件及申报流程
- [流程周期]保健食品注册申请条件及申报流程
- [流程周期]保健食品注册的法律界定、申报流程及资料要求
- [流程周期]保健食品备案信息填报流程图及备案资料形式要求
- [流程周期]天健华成小课堂:保健食品备案流程一览
- [流程周期]对改变产品名称、保质期、食用量,缩小适宜人群范围,扩大不适宜人群范围、注意事项以及功能项目的变更申请(进口)流程
- [流程周期]进口保健食品在境内转让流程图
- [流程周期]进口保健食品在境外转让流程图
- [流程周期]保健食品审批流程图
相关推荐:
- [申报攻略]进口化妆品申报注册备案系列之1:前言
- [政策法规]国家药监局发布《化妆品安全风险监测与评价管理办法》的公告(2025年第37号)
- [审批动态]2025年10月14日化妆品批准证明文件送达信息
- [审批动态]2025年06月11日化妆品批准证明文件(变更、纠错)送达信息
- [审批动态]2022年03月11日化妆品批准证明文件(HSCB)待领取信息发布
- [材料要求]首次进口化妆品申报注册备案之材料提供篇
- [常见问题]【答疑】上海器审|化妆品《产品名称命名依据》填报常见问题解答
- [审批动态]2024年03月28日化妆品注册批准证明文件送达信息发布
- [常见问题]江苏药监局审评中心化妆品备案注册你问我答问题汇总(2025年1季度)
- [政策法规]国家药监局关于进一步明确原特殊用途化妆品过渡期管理等有关事宜的公告(2021年 第150号)
化妆品申报频道
联系我们
-
86-010-84828041/42
400-6167-168
zhuceabc@zhuceabc.com
咨询微信:
13601366497(化妆品类)
1801335159(特殊食品类)
最新更新
热门排行